Cinematica degli enzimi: cos’è e a cosa serve?
Se siamo studenti di biologia ci sarà capitato di studiare la cinematica degli enzimi. In questo articolo capiremo a cosa serve e se siete in procinto di preparare un esame, avrete un po’ più chiara la sua utilità nel corpo umano.
Cosa sono gli enzimi?
Innanzitutto: gli enzimi sono proteine. Ma non proteine normali. Sono proteine altamente specializzate, fondamentali per poter svolgere i processi di liberazione di energia (ma non solo) in un lasso temporale utile per le richieste della cellula.
Gli enzimi aumentano la velocità di una reazione, sono specifici e non richiedono condizioni drastiche per poter funzionare, conciliandosi con la vita umana.
Nell’articolo “enzimi: struttura e funzioni” spiegammo in maniera sintetica anche altre nozioni.
Cos’è la cinematica enzimatica?
La cinematica enzimatica o cinetica enzimatica è lo studio delle reazioni chimiche permesse dagli enzimi. Molte molecole utili per la nostra vita, come per esempio la glicolisi, sono permesse grazie alla cinetica enzimatica.
L’equazione di primo ordine di cinetica enzimatica
Esistono molecole che interagiscono con gli enzimi che prendono il nome di substrati. Il substrato si lega all’enzima specifico e dopo un certo lasso di tempo si genera il prodotto della reazione.
La velocità di una reazione chimica è direttamente proporzionale alle concentrazioni del substrato. Esiste però una costante di velocità che non è altro che una costante di proporzionalità, chiamata k.
Il risultato sarà:
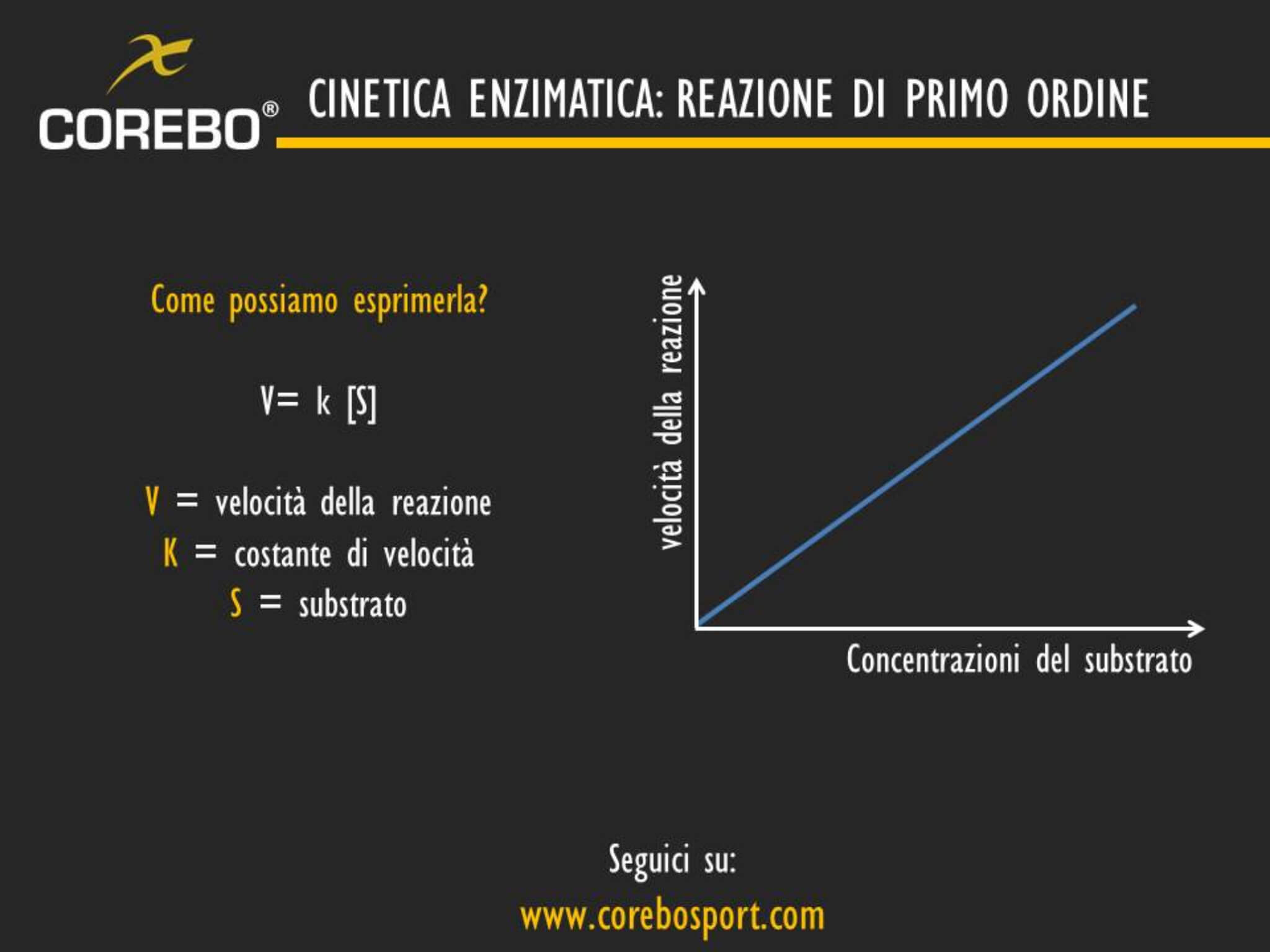
v=k[S]
Cosa significa?
La velocità della reazione è data dal prodotto tra la costante di velocità k e le concentrazioni del substrato, cioè la molecola che interagirà con l’enzima in questione.
Si genererà un grafico da questa equazione che non sarà altro che una retta. Questa viene chiamata reazione di primo ordine.
Quando si parla di reazione di secondo ordine?
La reazione di secondo ordine della cinetica enzimatica è molto semplice. Quando abbiamo due substrati, S1 e S2, l’equazione diventa automaticamente di secondo ordine. Questa può essere scritta nel seguente modo:
v=k[S1][S2]
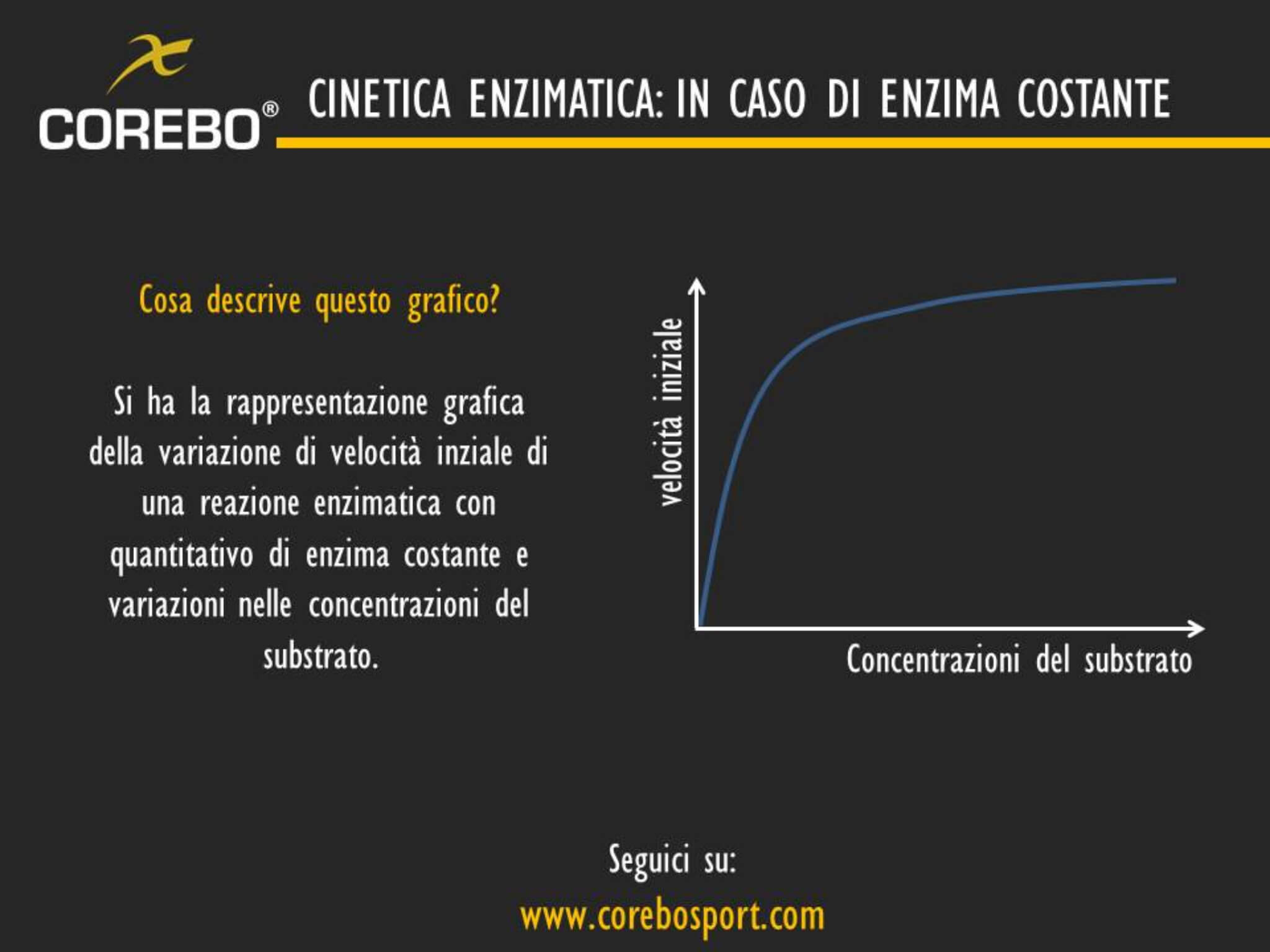
In verità se volessimo entrare molto più nella complessità cellulare la curva avrebbe un andamento iperbolico.
Inizialmente seguirebbe un andamento simile all’equazione di primo ordine, specie con basse concentrazioni del substrato.
Più le concentrazioni del substrato si alzano, più la velocità diventa completamente indipendente da esso. In questo caso si parla di reazione di ordine zero.
L’equazione di Michaelis e Menten e la cinematica enzimatica
E ora veniamo ad un altro paragrafo fondamentale per chi sta studiando gli enzimi e la cinetica enzimatica: l’equazione di Michaelis-Menten.
Questa equazione descrive il comportamento di una reazione dove sono coinvolti enzimi e in particolare la velocità iniziale in base alle concentrazioni del substrato.
Immaginiamo che l’equazione scritta nell’immagine diventi che la velocità iniziale è uguale alla metà della velocità massima. In questo caso avremo che la costante di Michaelis-Menten è uguale alle concentrazioni del substrato.
Km=[S]
Quando la costante rappresenta un valore basso, significa che si ha un’alta affinità tra enzima e substrato, come nel caso dell’esochinasi I.
Quando la costante di Michaelis-Menten ha un valore elevato, l’affinità tra enzima e substrato si abbassa notevolmente, come nel caso della glucochinasi o esochinasi IV.

A cosa serve conoscere queste nozioni?
Dallo studio della cinematica enzimatica sappiamo che gli enzimi hanno delle priorità differenti e il corpo riesce, in differenti situazioni, a veicolare i prodotti cellulari verso vie metaboliche ben precise.
Facciamo un esempio. Quando l’insulina è molto alta, si ha una principale attivazione dell’esochinasi IV, rispetto all’esochinasi I. Questo processo veicola il glucosio in eccesso nel torrente ematico, come nel caso del dopo-pranzo, per sintetizzare acidi grassi o nuovo glicogeno.
Invece nei periodi di digiuno avremo un’attivazione marcata dell’enzima esochinasi I che veicolerà il G6P (glucosio-6-fosfato) verso la glicolisi e il ciclo di Krebs.
Per gli studenti di biologia, conoscere tutto questo consente di comprendere molti aspetti del nostro corpo e molte vie metaboliche importanti: la via del pentoso-fosfato per esempio e altre accennate in questo articolo.
Buono studio!
A cura del Dr. Giulio Merlini
Tag:biochimica